Title
题目
A novel explainable AI framework for medical image classificationintegrating statistical, visual, and rule-based methods
一种集成统计、视觉和基于规则方法的新型可解释医学图像分类人工智能框架
01
文献速递介绍
人工智能(AI)和深度学习(DL)已彻底革新了需要高预测精度的领域,尤其是在医疗保健、刑事司法等高危应用场景中(Aamir 等人,2021)。近年来,在医疗领域,深度学习模型显著提升了多种成像模态的诊断准确性,包括磁共振成像(MRI)、胸片、组织病理学和超声检查等(Qayyum 等人,2024;Ullah 等人,2023)。尽管取得了成功,但这些模型因缺乏透明度和可解释性而受到批评,引发了信任和伦理方面的担忧,尤其是在医疗保健等关键领域(Rudin,2019;Poon 和 Sung,2021)。 为应对这些挑战,可解释人工智能(XAI)和可解释人工智能(IAI)应运而生(Ullah 等人,2024a)。XAI 技术用于解释深度学习模型的决策逻辑,在不牺牲准确性的前提下增强透明度和信任度。事后 XAI 方法,如特征重要性排名(Wojtas 和 Chen,2020)、显著性图(Gomez 等人,2022)和基于梯度的可视化(Selvaraju 等人,2017),旨在为黑箱模型提供洞察。相比之下,IAI 开发本质上透明的模型,如决策树或基于规则的系统,以人类可读的格式呈现决策过程(Reyes 等人,2020;De Falco 等人,2023)。 然而,仍存在一些关键局限性。尽管卷积层提取的深度特征对分类有效,但其具有抽象性,缺乏对专家的语义互操作性,难以理解特定特征如何影响决策。此外,大多数可视化方法(如显著性图)仅突出显示与预测相关的一般输入区域,无法提供详细的特征级解释。基于规则的方法往往缺乏与视觉解释的集成,导致见解碎片化。这种脱节在医疗保健领域尤为突出,因为透明和精确的解释对信任和决策至关重要。 为解决这些问题,本研究提出了统计、视觉和基于规则的可解释框架(SVIS - RULEX)。这个新框架集成了统计、视觉和基于规则的解释,用于解释基于深度学习的模型在应用于医学图像时如何做出决策。与传统方法不同,该框架将深度特征转换为可解释的统计属性,实现可追溯和可量化的预测。此外,还引入了一种称为 SFMOV 的新方法。SFMOV 通过将统计量(如均值、偏度、熵)叠加到特征图上,增强了可视化效果,提供了局部化和特定于特征的见解。通过融合统计、视觉和基于规则的解释,该方法确保了更高的透明度和可解释性,这对医疗应用至关重要。 为验证 SVIS - RULEX 框架的鲁棒性和通用性,在来自 Kaggle 的五个不同医学成像数据集上进行了评估,涵盖胸片、乳腺超声、脑部 MRI、组织病理学和眼底图像。这一广泛的评估证明了该框架在各种成像模态和医疗状况下的适应性和有效性。 本研究的主要贡献总结如下: 1. 采用双路径方法,集成视觉和基于规则的解释,在保持分类性能的同时增强可解释性。 2. 使用定制的 MobileNetv2 模型进行深度特征提取,从各种医学成像模态中捕获高维表示。 3. 引入新颖的统计特征工程方法,从深度特征生成 26 个人类可读的属性(如均值、方差、偏度、熵),以提高可解释性。 4. 开发新的 ZFMIS 策略用于特征排名和选择,确保特征集紧凑且信息丰富。 5. 使用决策树(DT)和 RuleFit 进行基于规则的解释,为模型的决策过程提供人类可理解的见解。 6. 提出新的 SFMOV 技术,可视化卷积特征的统计叠加(均值、偏度、熵),并通过密集层属性加权,以实现更深入的解释。 7. 与放射科医生对 SFMOV 可视化进行临床验证,确认其诊断相关性和实际意义。 论文的其余部分结构如下:第 2 节回顾相关工作;第 3 节详细介绍所提出的方法;第 4 节展示和讨论结果;第 5 节总结全文。
Abatract
摘要
Artificial intelligence and deep learning are powerful tools for extracting knowledge from large datasets,particularly in healthcare. However, their black-box nature raises interpretability concerns, especially in highstakes applications. Existing eXplainable Artificial Intelligence methods often focus solely on visualization orrule-based explanations, limiting interpretability’s depth and clarity. This work proposes a novel explainableAI method specifically designed for medical image analysis, integrating statistical, visual, and rule-basedexplanations to improve transparency in deep learning models. Statistical features are derived from deepfeatures extracted using a custom Mobilenetv2 model. A two-step feature selection method – zero-basedfiltering with mutual importance selection – ranks and refines these features. Decision tree and RuleFit modelsare employed to classify data and extract human-readable rules. Additionally, a novel statistical feature mapoverlay visualization generates heatmap-like representations of three key statistical measures (mean, skewness,and entropy), providing both localized and quantifiable visual explanations of model decisions. The proposedmethod has been validated on five medical imaging datasets – COVID-19 radiography, ultrasound breast cancer,brain tumor magnetic resonance imaging, lung and colon cancer histopathological, and glaucoma images – withresults confirmed by medical experts, demonstrating its effectiveness in enhancing interpretability for medicalimage classification tasks
人工智能和深度学习是从大型数据集中提取知识的强大工具,尤其在医疗保健领域。然而,其“黑箱”特性引发了可解释性方面的担忧,特别是在高风险应用场景中。现有的可解释人工智能方法往往仅专注于可视化或基于规则的解释,限制了可解释性的深度和清晰度。这项工作提出了一种专为医学图像分析设计的新型可解释人工智能方法,该方法集成了统计、视觉和基于规则的解释,以提高深度学习模型的透明度。 统计特征源自使用定制MobileNetV2模型提取的深层特征。通过基于零的过滤与互信息选择相结合的两步特征选择方法,对这些特征进行排序和优化。决策树和RuleFit模型用于对数据进行分类并提取人类可读的规则。此外,一种新颖的统计特征图叠加可视化技术可生成类似热图的三种关键统计量(均值、偏度和熵)表示,为模型决策提供局部化和可量化的视觉解释。 该方法已在五个医学成像数据集上得到验证,包括COVID-19放射影像、超声乳腺癌图像、脑肿瘤磁共振图像、肺和结肠癌组织病理学图像以及青光眼图像。医学专家对结果的确认表明,该方法在增强医学图像分类任务的可解释性方面具有有效性。
Method
方法
This work integrates rule-based modeling and visualizations withstatistical feature engineering and DL-based feature extraction to produce human-understandable explanations. This method bridges thegap between interpretable techniques’ transparency and black-box DLmodels’ predictive power. Fig. 1 shows an overview of the proposedmethod. First, some existing techniques are used in preprocessing, likedata augmentations, image resizing, and region of interest cropping.The resultant dataset is then fed into the custom MobileNetv2 DL modelfor feature extraction to capture complex visual patterns and get morediscriminative and informative deep features, which are crucial foraccurate classification. These extracted features are then used for statistical transformation to compute interpretable, summary-level insights.Next, a novel ZFMIS technique ranks and filters features based on theirinterpretive value. The filtered and selected features are then used totrain the decision tree and RuleFit interpretable rule-based models. Finally, Grad-CAM-inspired heatmaps (SFMOV) are generated to visualizethe most important statistical features and highlight spatial regions ofthe images that contribute significantly to the model’s decision-makingprocess. Visual overlays enhance statistical interpretation by illustrating how specific patterns affect categorization judgments, providingstakeholders with an intuitive understanding of the prediction model’sbehavior, a model-agnostic visual explanation technique.The pseudocode of the proposed methodology is presented in Algorithm 1. Each step is discussed in detail in the subsequent sections.
本研究将基于规则的建模与可视化,同统计特征工程和基于深度学习的特征提取相结合,以生成人类可理解的解释。该方法弥合了可解释技术的透明度与黑箱深度学习模型预测能力之间的差距。图1展示了所提方法的概述。首先,预处理阶段采用了一些现有技术,如数据增强、图像Resize和感兴趣区域裁剪。随后,将处理后的数据集输入定制的MobileNetv2深度学习模型进行特征提取,以捕获复杂的视觉模式并获取更具判别性和信息量的深度特征,这些特征对精确分类至关重要。 接下来,所提取的特征会进行统计变换,以计算具有可解释性的概要级洞察。然后,一种新颖的ZFMIS技术会基于特征的解释价值对其进行排序和过滤。经过筛选的特征将用于训练决策树和RuleFit等可解释的基于规则模型。最后,生成受Grad - CAM启发的热图(SFMOV),以可视化最重要的统计特征,并突出显示图像中对模型决策过程有显著贡献的空间区域。可视化叠加通过展示特定模式如何影响分类判断来增强统计解释,为利益相关者提供对预测模型行为的直观理解,这是一种与模型无关的可视化解释技术。 所提方法的伪代码见算法1,后续章节将详细讨论每个步骤。
Conclusion
结论
This study proposed SVIS-RULEX as an innovative framework toenhance the interpretability of deep learning models, particularly forcritical applications in healthcare. By combining statistical feature engineering, rule-based modeling, and visual overlays, the methodologyaddresses key limitations of existing XAI approaches, offering a holisticsolution for interpreting black-box models in medical diagnostics.The framework demonstrated the ability to provide transparent,interpretable insights without compromising predictive performance.By integrating statistical metrics such as mean, skewness, and entropy,the method enriched the interpretive capacity of deep learning models,while ZFMIS effectively reduced dimensionality, preserving only themost critical features. This approach facilitated the development ofinterpretable and high-performing models, offering valuable insightsinto the underlying patterns and decision-making processes of themodel.Visual overlays generated by SFMOV provided meaningful heatmaps,highlighting diagnostically relevant areas and demonstrating the model’sfocus on critical regions within medical images. These visualizationssupported clinical trust in the decision-making process, ensuring thatthe results were interpretable and actionable.The versatility of the framework was evident in its ability to performconsistently across a variety of medical imaging modalities, includingradiographs, ultrasounds, and histopathological images. This scalabilityemphasizes its potential for broad application in diagnostics, makingit particularly valuable in high-stakes domains like healthcare. Importantly, the rule-based explanations offered by decision trees andRuleFit models bridged the gap between computational predictions andhuman understanding, enabling a clearer interpretation of the model’sdecision-making process.The study not only highlights the proposed framework’s interpretability and transparency but also establishes its relevance forimproving trust and adoption in realworld clinical settings.Despite its promising contributions, the proposed SVIS-RULEX framework has certain limitations. While the rule-based explanations provideclarity, they might oversimplify the underlying decision-making process of deep learning models, potentially missing nuanced patternsthat contribute to predictions. The reliance on visual heatmaps forinterpretability also assumes that the highlighted regions fully capturediagnostically relevant features, which may not always align withdomain experts’ expectations. Furthermore, the framework’s evaluationfocused on specific imaging modalities and datasets, raising the needfor extensive validation across broader, more heterogeneous datasetsto ensure its generalizability.It is worth noting that SFMOV does not necessarily coincide exactlywith clinically marked tumor or consolidation areas. While these regions often overlap with areas typically examined by human expertsduring diagnosis, it is important to note that XAI methods, such asSFMOV, are not designed to exactly replicate expert attention. Instead, they may capture subtle, discriminative patterns that inform themodel’s decisions but do not always align with clinically defined tumoror consolidation boundaries.The current SFMOV approach employs statistical feature maps(mean, skewness, entropy), computed directly from the original activation maps of the final convolutional layer without applying additionallearned or domain-specific weights. This deliberate choice preservesthe direct interpretability of the features of the learned model andavoids introducing external bias, ensuring that the visualizations remain faithful to the representations of the inherent features of thenetwork. Although this method is computationally efficient and effectively highlights regions of model attention, the absence of learnedweighting may result in broader, less localized feature activations.However, integrating the learned weights could improve visualizationclarity while preserving the integrity of the model.Furthermore, another limitation of the proposed method is that, forsome data sets, the SFMOV combined heatmaps are visually very closeto the mean heatmap. This closeness means that the effect of the meanfeature can dominate the visualization and could undermine the contribution of skewness and entropy under such scenarios. Future workwill focus on addressing this limitation by enhancing the weighting ofstatistical features in a way that makes the discrimination higher incombined heatmaps.Finally, the computational overhead introduced by combining statistical, rule-based, and visual methods may pose challenges for realtime deployment in resource-constrained settings. Addressing these limitations in future work will be essential to further enhance the framework’s robustness and applicability in diverse and practical clinicalenvironments.
本研究提出了SVIS-RULEX这一创新框架,以增强深度学习模型的可解释性,尤其是在医疗领域的关键应用中。通过结合统计特征工程、基于规则的建模和可视化叠加,该方法解决了现有可解释人工智能(XAI)方法的关键局限性,为医学诊断中黑箱模型的解释提供了整体解决方案。 该框架展示了在不影响预测性能的情况下提供透明、可解释见解的能力。通过集成均值、偏度和熵等统计指标,该方法丰富了深度学习模型的解释能力,而ZFMIS(零基过滤与互信息选择)则有效降低了维度,仅保留最关键的特征。这种方法促进了可解释且高性能模型的开发,为理解模型的潜在模式和决策过程提供了有价值的见解。 SFMOV(统计特征图叠加可视化)生成的可视化叠加提供了有意义的热图,突出了诊断相关区域,并展示了模型对医学图像中关键区域的关注。这些可视化支持了临床对决策过程的信任,确保结果具有可解释性和可操作性。 该框架的多功能性体现在其能够在各种医学成像模式(包括放射影像、超声和组织病理学图像)中一致表现。这种可扩展性强调了其在诊断中的广泛应用潜力,使其在医疗等高风险领域特别有价值。重要的是,决策树和RuleFit模型提供的基于规则的解释架起了计算预测与人类理解之间的桥梁,使模型的决策过程能够更清晰地被解读。 这项研究不仅强调了所提出框架的可解释性和透明度,还确立了其在现实临床环境中提高信任度和采用率的相关性。 尽管有这些有希望的贡献,所提出的SVIS-RULEX框架也存在一定的局限性。虽然基于规则的解释提供了清晰度,但它们可能会简化深度学习模型的潜在决策过程,有可能忽略对预测有贡献的细微模式。依赖可视化热图进行解释还假定突出显示的区域完全捕获了诊断相关特征,但这可能并不总是与领域专家的期望一致。此外,该框架的评估侧重于特定的成像模式和数据集,因此需要在更广泛、更多样化的数据集上进行广泛验证,以确保其通用性。 值得注意的是,SFMOV不一定与临床标记的肿瘤或实变区域完全一致。尽管这些区域通常与人类专家在诊断过程中检查的区域重叠,但需要注意的是,像SFMOV这样的XAI方法并不是为了完全复制专家的关注点而设计的。相反,它们可能捕获为模型决策提供信息的微妙判别模式,但这些模式并不总是与临床定义的肿瘤或实变边界一致。 当前的SFMOV方法采用直接从最终卷积层的原始激活图计算的统计特征图(均值、偏度、熵),而不应用额外的学习权重或领域特定权重。这一慎重选择保留了所学模型特征的直接可解释性,并避免引入外部偏差,确保可视化忠实于网络固有特征的表示。尽管这种方法计算效率高,并能有效突出模型关注的区域,但缺乏学习权重可能会导致更广泛、定位更差的特征激活。不过,集成学习权重可以在保持模型完整性的同时提高可视化的清晰度。 此外,该方法的另一个局限性是,对于某些数据集,SFMOV组合热图在视觉上与均值热图非常接近。这种接近意味着均值特征的影响可能在可视化中占主导地位,在这种情况下可能会削弱偏度和熵的贡献。未来的工作将专注于解决这一局限性,通过增强统计特征的权重,使组合热图中的区分度更高。 最后,结合统计、基于规则和可视化方法所带来的计算开销,可能会给资源受限环境下的实时部署带来挑战。在未来的工作中解决这些局限性,对于进一步增强该框架在不同实际临床环境中的鲁棒性和适用性至关重要。
Results
结果
This section introduces information about the experiments performed and the results produced in this study. This section also provides additional information about the datasets, experimental setup,optimized hyper-parameters, and evaluation metrics used in this study.4.1. DatasetsThis study uses five publicly available Kaggle datasets with various medical imaging modalities to assess the proposed approach’sgeneralizability and robustness across distinct medical conditions. Thefive datasets are well-known datasets, and each covers diverse diseases, imaging techniques, and anatomical regions. The summary of thedatasets is given in Table 3 whereas the representative samples fromthese datasets are given in Fig. 3.
本节介绍了本研究中进行的实验及产生的结果相关信息,还提供了关于数据集、实验设置、优化的超参数以及本研究中使用的评估指标的额外信息。 ### 4.1 数据集 本研究使用了五个可从Kaggle获取的公开数据集,这些数据集具有不同的医学成像模态,以评估所提出方法在不同医疗状况下的通用性和鲁棒性。这五个数据集均为知名数据集,每个数据集涵盖了不同的疾病、成像技术和解剖区域。数据集的概述见表3,而这些数据集的代表性样本见图3。
Figure
图

Fig. 1. Workflow of the proposed approach.
图1. 所提方法的工作流程。

Fig. 2. SFMOV process, extracting Mean, Skewness, and Entropy maps from convolutional features and dense layer activations, normalizing and combining them into a weightedheatmap overlaid on the input imag
图2. SFMOV流程,从卷积特征和密集层激活中提取均值、偏度和熵图,对其进行归一化并组合成加权热图,叠加在输入图像上。

Fig. 3. Representative samples from all datasets, first, second, third, fourth, and fifth columns have representative samples from dataset 1, dataset 2, dataset 3, dataset 4, anddataset 5, respectively
图3. 所有数据集的代表性样本,第一、第二、第三、第四和第五列分别为数据集1、数据集2、数据集3、数据集4和数据集5的代表性样本。

Fig. 4. SFMOV-based heatmap visualization showing a COVID-19 image detected as COVID-19 (row 1) and a COVID-19 image detection as viral pneumonia (row 2). Red arrowsindicate consolidation and blue arrows indicate healthy parenchyma (the latter is what is focused on)
图4. 基于SFMOV的热图可视化,显示被检测为COVID-19的图像(第一行)和被检测为病毒性肺炎的COVID-19图像(第二行)。红色箭头指示实变区域,蓝色箭头指示健康肺实质(后者为关注重点)。

Fig. 5. SFMOV-based heatmap visualization showing a malignant ultrasound image detected as malignant (row 1) and a benign ultrasound image detection as benign (row 2).Red arrows represent the abrupt interface between healthy tissue and tumor
图5. 基于SFMOV的热图可视化结果:第一行为被正确识别为恶性的超声图像,第二行为被正确识别为良性的超声图像。红色箭头标注了健康组织与肿瘤之间的边界突变区域。

Fig. 6. SFMOV-based heatmap visualization showing a malignant image predicted as malignant (row 1) and a malignant image predicted as benign (row 2). Red arrows indicatethe healthy tissue/healthy interface, while blue arrows indicate the tumor/lesion.
图6. 基于SFMOV的热图可视化:第一行为被正确预测为恶性的图像,第二行为被误判为良性的恶性图像。红色箭头指向健康组织/健康边界,蓝色箭头指向肿瘤/病变区域。

Fig. 7. SFMOV-based heatmap visualization showing a colon adenocarcinoma image predicted as colon adenocarcinoma (row 1) and a benign colon image predicted as benigncolon (row 2). The pathological area is indicated by the blue arrow, whereas the red arrow indicates the healthy tissue/the transition zone.
图7. 基于SFMOV的热图可视化结果:第一行为被正确预测为结肠腺癌的图像,第二行为被正确预测为良性结肠组织的图像。蓝色箭头标注病理区域(癌变部位),红色箭头指示健康组织/过渡区。

Fig. 8. SFMOV-based heatmap visualization showing a glaucoma image (row 1) and a normal image (row 2), both correctly classified, with model focus on clinically relevantoptic nerve regions. Red arrows indicate the macular zone, while blue ones are the transition zone with the non-macular area
图8. 基于SFMOV的热图可视化结果:第一行为正确分类的青光眼图像,第二行为正确分类的正常图像,模型聚焦于临床相关的视神经区域。红色箭头标注黄斑区,蓝色箭头指示黄斑区与非黄斑区的过渡带。
Table
表

Table 1Statistical feature descriptions and formulas
表1 统计特征描述及公式

Table 2Hyperparameters values for each model used in grid search optimization.
表2 网格搜索优化中各模型的超参数值

Table 3Summary of the datasets used in this study
表3 本研究中使用的数据集概述

Table 4Experimental setup: Software and hardware specifications
表4 实验设置:软件和硬件规格

Table 5Summary of the optimized hyperparameters on each dataset.
表5 各数据集上优化超参数概述

Table 6Top three selected features from 26 features set for each dataset based on MI after employing two-stage feature selection algorithm (ZFMIS).
表6 基于两阶段特征选择算法(ZFMIS)应用后,根据互信息(MI)为每个数据集从26个特征集中选出的前三特征。

Table 7Classification results of COVID-19 Radiography Database on a comprehensive set of statistical features with varying feature counts for DT andRuleFit
表7 COVID-19放射影像数据库在使用不同特征数量的综合统计特征集时,决策树(DT)和RuleFit的分类结果。

Table 8Classification results of Ultrasound Breast Images for Breast Cancer on a comprehensive set of statistical features with varying feature countsfor DT and RuleFit.
表8 乳腺癌超声图像数据集在使用不同特征数量的综合统计特征集时,决策树(DT)和RuleFit的分类结果。
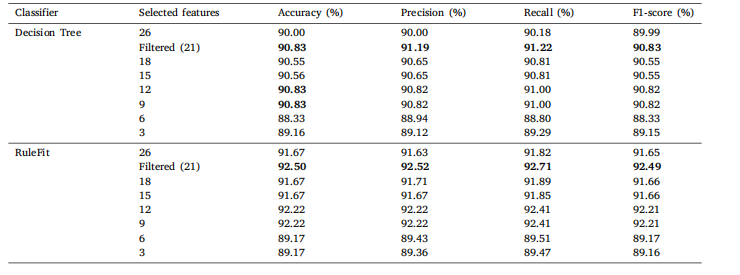
Table 9Classification results of Brain MRI Images for Brain Tumor Detection on comprehensive set of statistical features with varying feature countsfor DT and RuleFit
表9 脑肿瘤检测用脑部MRI图像数据集在采用不同特征数量的综合统计特征集时,决策树(DT)和RuleFit的分类结果。

Table 10Classification results of Lung and Colon Cancer Histopathological Images on the comprehensive set of statistical features with varying featurecounts for DT and RuleFit
表10 肺癌和结肠癌组织病理学图像数据集在使用不同特征数量的综合统计特征集时,决策树(DT)和RuleFit的分类结果。

Table 11Classification results of ACRIMA from Generated Eye Dataset for Glaucoma Detection on the comprehensive set of statistical features withvarying feature counts for DT and RuleFit
表11 青光眼检测用生成眼部数据集(ACRIMA)在采用不同特征数量的综合统计特征集时,决策树(DT)和RuleFit的分类结果。

Table 12Decision tree rules for top two datasets based on classification performance
表12 基于分类性能的前两个数据集的决策树规则

Table 13RuleFit rules for top two datasets based on classification performance
表13 基于分类性能的前两个数据集的RuleFit规则

Table 14Classification performance of different noninterpretable approaches across multiple datasets
表 14 不同非可解释方法在多数据集上的分类性能
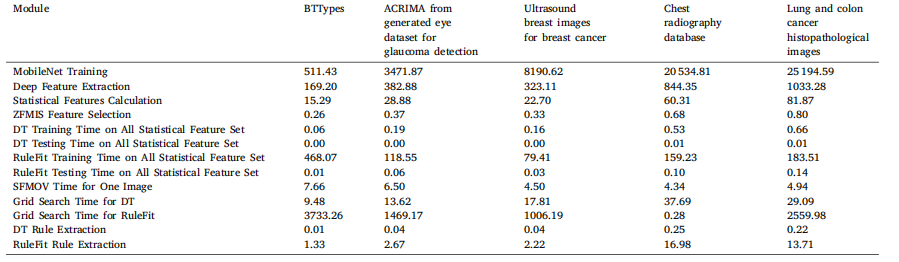
Table 15Computation time (in Seconds) for different modules on multiple datasets.
表 15 不同模块在多个数据集上的计算时间(秒)
![洛谷 P10113 [GESP202312 八级] 大量的工作沟通-普及/提高-](http://pic.xiahunao.cn/洛谷 P10113 [GESP202312 八级] 大量的工作沟通-普及/提高-)


)


C++函数新特性——函数重载)









的python脚本)


